NAI: .3-6-3.
Tema Eje: Relaciones de Masa en las Reacciones Químicas.
Línea de acción: Agua y Sustancias Químicas.
Región: Lima Este
Actividad: Día de las Américas.
Categoría: Manejo Ambiental
USO DEL HIDRÓGENO OBTENIDO A PARTIR DE UNA REACCIÓN ENTRE EL GALIO Y EL ALUMINIO, COMO COMBUSTIBLE, PARA DISMINUIR LA CONTAMINACION EN LIMA ESTE.
Objetivo(s):-Disminuir la contaminación en Lima Este.
- Usar el hidrógeno como combustible en los automóviles.
- Producir el hidrógeno a partir de una reacción entre el galio y el aluminio
Variables:
Variable independiente: Producción del hidrógeno como combustible a partir de una reacción entre el galio y el aluminio.
Variable dependiente: Disminución de la contaminación ambiental.
Hipótesis: El uso del hidrógeno obtenido a partir de una reacción entre el galio y el aluminio, como combustible, disminuye la contaminación ambiental en Lima Este.
Resumen (250 palabras): Las principales causas de la contaminación del aire están relacionadas con la quema de combustibles fósiles (carbón, petróleo y gas). La combustión de estas materias primas se produce en los procesos o en el funcionamiento de los sectores industrial y del transporte por carretera, principalmente.
El uso del hidrógeno obtenido a partir de una reacción entre el Galio y el Aluminio, como combustible, puede disminuir el índice contaminación en aire de la Subregión Lima Este.
Este informe tiene como objetivo plantear el uso del hidrógeno obtenido a partir de una reacción entre el Galio y el Aluminio para reducir la contaminación generada por la población automovilística.
El galio es un componente muy importante ya que impide la formación de una película de óxido sobre el aluminio. Esto suele aparecer en la superficie del aluminio durante la oxidación y actúa como barrera, no dejando que el oxigeno reaccione con el aluminio. Reduciendo esta película protectora, la reacción sigue su curso hasta que todo el aluminio es usado para generar hidrógeno. Además, el galio es un componente inerte, lo que quiere decir que puede ser recuperado y reutilizado. El proceso funciona de la siguiente manera: cuando se mezclan agua y unas pequeñas bolas de una aleación de aluminio/galio, el agua y el aluminio reaccionan y se forma óxido de aluminio, lo cual libera el hidrógeno. Esta reacción es violenta y muy exotérmica, de modo que en el uso cotidiano del dispositivo, el agua se añadiría poco a poco al aluminio. Al ser la reacción tan rápida, es posible generar hidrógeno bajo demanda, es decir, producir la reacción según se necesite utilizar el gas en vez de tener que transportarlo como ahora. El galio es importante por dos razones: en primer lugar, el aluminio sólido no reacciona espontáneamente con agua (o nuestras cocinas serían trampas mortales), pero cuando está aleado con galio sí lo hace. Además, el galio evita que, según el aluminio va reaccionando con el agua, se forme una capa de óxido de aluminio sobre la superficie de la bola y la reacción se detenga. Con el galio, la bola reacciona completamente. Cuando la reacción ha terminado, lo que se tiene por un lado es óxido de aluminio con galio (que no se gasta ni sufre ninguna transformación permanente, ya que está actuando de catalizador), y por otro, hidrógeno.
Problema: Esta región presenta una alta contaminación por: Monóxido de Carbono (CO), Dióxido de Azufre (SO2), Plomo (PB), Óxidos de Nitrógeno (NO, NO2), Sulfuros de Hidrogeno (SH2), etc. Principalmente estos GEI (Gases de Efecto Invernadero) son producidos por la quema de combustibles fósiles, la producción de fabricas, producción de energía, etc.
Solución: Esta Reacción entre el Galio y el Aluminio produce Hidrogeno, lo que actualmente se está usando en países avanzados por ser una tecnología renovable, esta solución es muy efectiva ya que el Hidrogeno es el gas más abundante en la Tierra y que por muchos años no ha sido de mucha contaminación para la capa de ozono.
Conclusiones: Se comprobó la hipótesis, ya que el uso de él hidrogeno obtenido a partir de una reacción entre el galio y el aluminio, como combustible, disminuye la contaminación ambiental en Lima Este ya que es muy efectiva y de bajo costo.
Fotos:
Procedimiento de obtención del hidrogeno.
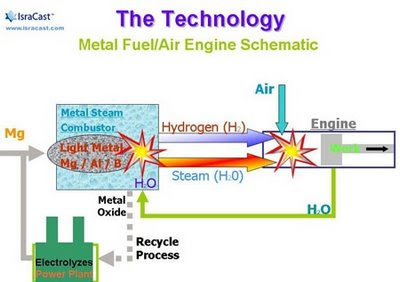
Carro a Hidrogeno.

Estadisticas:
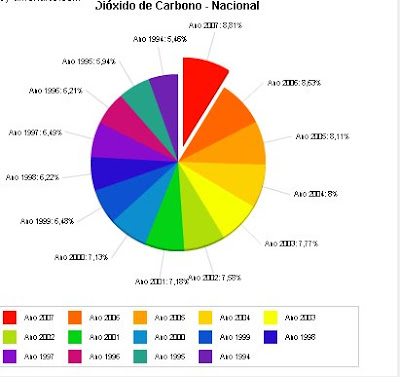
Investigación futura: Investigar si aparte de este proceso de producción de hidrogeno haya otro que mejore las expectativas y supere la reducción de gases contaminantes.
Alfabetización funcional (FODA):
Fortalezas: El costo del Hidrogeno como combustible es bajo.
Oportunidades: Reducir la emisión de gases contaminantes.
Debilidades: Cambio radical de motores de los autos.
Amenazas: Apoyo de esta Subregión, por parte económica y financiera.
Origen y motivo de la investigación: Este proyecto me proyecto me intereso por la contaminación que observamos y percibimos en cada paso que damos en las calles, cada ves que pasamos por la Av. Abancay, se nota la contaminación en la que personas viven y realizan trabajos aspirando cantidades incontables de agentes contaminantes.
Viabilidad a la región: Este proceso puede interesar a la mayoría de los pobladores para reducir el costo por lo que normalmente pagan por un combustible fósil , dentro de ello la gasolina el más usado que es un derivado del petróleo , este proceso tiene sus ventajas y desventajas :
Ventajas
-No libera dióxido de carbono
-El quemar hidrogeno podría eliminar la mayor parte de la contaminación del agua y del aire causada por la extracción, el transporte y quema de combustibles fósiles y podría reducir en gran medida la amenaza del calentamiento planetario.
-La energía nuclear podría discontinuarse.
Desventajas
-El principal problema del hidrogeno es que solo existen cantidades mínimas o trazas del gas en la naturaleza.
-Su producción requiere de calor de temperatura elevada o de electricidad producidos por otra fuente de energía, como fisión nuclear, la energía solar directa o del viento, para descomponer el agua.
-La producción de hidrógeno mediante cualquier método requiere más energía de la que se libera cuando arde o se quema. De este modo, su producción de energía útil neta siempre será negativa, lo que significa que la generalización de su uso depende de contar con un suministro abundante y permisible de algún tipo de energía ambientalmente aceptable.
Palabras claves (Definición)
-Hidrogeno: Elemento químico representado por el símbolo H y con un número atómico de 1.
-Reacción Exotérmica: Es cualquier reacción química que desprende calor, es decir con una variación negativa de entalpía.
-Catalizador: Es la sustancia que en un proceso llamado catálisis, modifica la velocidad de una reacción química.
-Aluminio: Elemento químico, de símbolo Al y número atómico 13.
-Galio: Elemento químico de la tabla periódica de número atómico 31 y símbolo Ga.
Datos Personales:
Apellidos y Nombres: Olave Jaime Renzo
Año de estudios: 3er sec
Nodo: Minicientificos
Correo electrónico: renzoolave2010@gmail.com
